シクロアミロース™
シクロアミロース
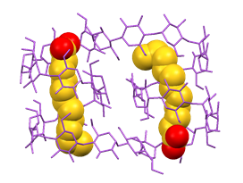
シクロアミロースは、17~数百個のブドウ糖が環状につながった環状α-1,4-グルカンです。へリックス構造の内側に、立体的で奥行きのある空洞(中空)部分を有しています。
シクロアミロースが、タンパク質のリフォールディングにおいて、人工シャペロン(※1)として機能することを、独立行政法人 農業・食品産業技術総合研究機構 食品総合研究所と江崎グリコが共同で明らかにしました。
一般用途のシクロアミロース試薬は、富士フイルム和光純薬(株)より販売されています。なお一般用途のシクロアミロース試薬をタンパク質リフォールディング用途にご使用になる場合は、別途ライセンスが必要となります。
研究用途以外でシクロアミロースをご利用になる場合は、グリコ栄養食品にお問い合わせください。
※1 人工シャペロン
タンパク質は、正しい立体的構造をとるように折りたたまれる(フォールディング)ことにより、機能を発揮します。生物の細胞の中には、タンパク質の正しいフォールディングを進行させるためのシステムがあり、これを分子シャペロンといいます。この細胞の中のフォールディング過程を、試験管内で人工的に再現させるために利用する物質が人工シャペロンです。
【参考文献】
- S. Machida et al., FEBS Letters, 486, 131-135 (2000).
構造および製造方法
シクロアミロースは、17~数百個のブドウ糖が環状につながった環状α-1,4-グルカンです。へリックス構造の内側に、立体的で奥行きのある空洞(中空)部分を有しています。
デンプンに江崎グリコが開発した酵素「アミロマルターゼ」を作用させて製造します。
【参考文献】
- Y. Terada et al., Appl. Environ. Microbiol.,65 (3), 910-915 (1999).
- K. Gessler et al., PNAS,96, 4246-4251 (1999).
- W. Saenger et al., Chem. Rev.,98, 1787-1802 (1998).
上の図で、灰色はブドウ糖単位の2位と3位の酸素原子を、 黄色は6位の炭素原子をあらわしています。
構造を分かりやすくするために、他の原子は省略してあります。

特長
水溶性が高い
親水性高分子であるため、冷水に容易に溶解します。
加温により0.3g/ml以上溶解します。水溶液の安定性が高い
ただし、溶液で保存する場合、無菌状態での保存をおすすめします。包接能を持つ
ヘリックス構造などの立体構造中の疎水性空洞内にゲスト化合物を包接することができます。
包接により、ゲスト化合物の可溶化、安定化、徐放など、物理化学的性質を変えることができます。
(1)シクロアミロースと界面活性剤の相互作用の解析
シクロアミロースと界面活性剤との複合体形成は、シクロアミロースの重合度により異なります。
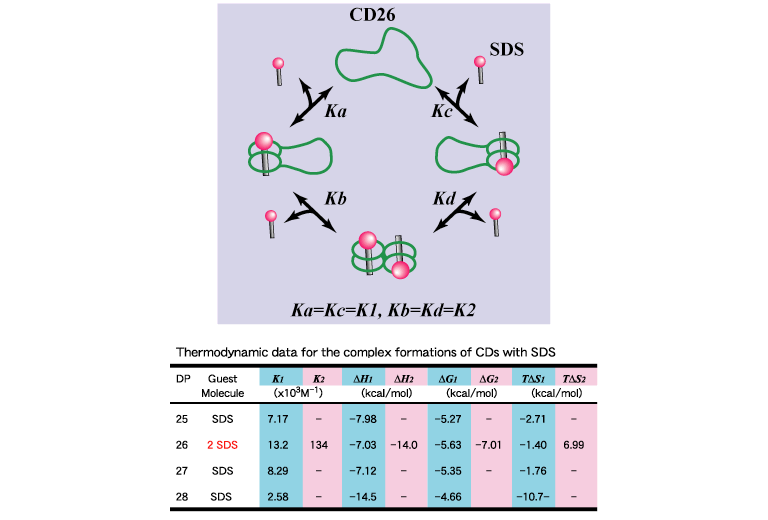
単一重合度に精製したシクロアミロースと界面活性剤(SDS)との相互作用を滴定型等温カロリメトリー法により解析したところ、重合度26のシクロアミロースはSDSと2:1の強い複合体を形成するのに対し、重合度25、27、28のものはSDSと1:1の複合体を形成しました。また、界面活性剤の種類を変えると、異なる重合度のシクロアミロースが強く相互作用します。
リフォールディングに用いているシクロアミロースの重合度分布は、22~50程度と幅があり、様々な種類の界面活性剤を包接することができると考えられます。
シクロアミロースと界面活性剤との相互作用の解析
【参考文献】
- 北村進一 応用糖質科学会誌 50 (2), 321-325 (2003).
(2)シクロアミロースと脂肪酸または高級アルコールとの包接
重合度26のシクロアミロースとウンデカン酸(C10H21COOH)およびドデカノール(C21H25OH)との包接複合体のX線結晶構造解析についても、すでに明らかになっています。
【参考文献】
- O. Nimz et al., Carbohydr. Res., 339, 1427-1437 (2004).
タンパク質リフォールディングの仕組み
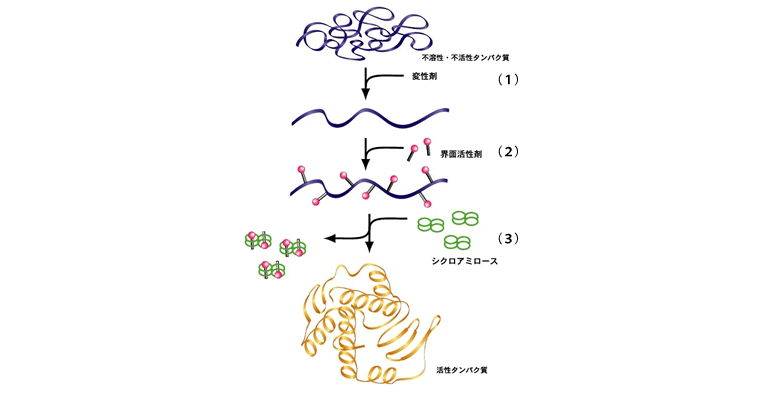
- 機能を失った不活性・不溶性の凝集タンパク質を、塩酸グアニジンなどの変性剤によって、立体構造を解きほぐし可溶化します。
- 次に、界面活性剤を含む溶液を加え希釈します。これにより、変性剤の濃度を下げると共に、タンパク質が再度凝集することを防ぎます。
- 最後に反応液にシクロアミロースを添加すると、正しい立体構造を取り戻した機能を有する活性なタンパク質になります。
このことから、シクロアミロースの包接作用によりタンパク質に結合している界面活性剤が徐々に取り除かれながら、リフォールディングが行われるものと推測されます。
参考資料
<1>リフォールディングプロトコール (1gのシクロアミロース(CA)を使用した場合)
(1) 封入体(inclusion body, 3~30 mg) を適当な緩衝液 ( 450 μl ) に懸濁
↓
(2) 8M塩酸グアニジン( 1.4 ml ) と4M DTT ( 19 μl )を加え、室温1時間~一晩放置
↓
(3) 界面活性剤液*( 130 ml) を加え、室温1時間放置
*界面活性剤液:界面活性剤(下記リフォールディング例参照)を終濃度0.05~0.12%となるように緩衝液に溶解したもので、必要に応じてDL-cystineを終濃度2mMとなるように加える。
↓
(4) 1g CAを33mlの水に溶解して加え、室温一晩放置
↓
(5) 沈殿を除去し、上清をリフォールドされたタンパク質溶液として回収
<2>シクロアミロースを用いた各種タンパク質のリフォールディング例
| 対象タンパク質 | 界面活性剤 | 活性回復率(%) |
|---|---|---|
| Citrate Synthase | Tween40 | 100 |
| Tween60 | 100 | |
| Carbonic Anhydrase B | CTAB | 92.7 |
| SB3-14 | 82.1 | |
| Lysozyme | CTAB | 91.8 |
| SB3-14 | 85.2 |
【参考文献】
- S. Machida et al. FEBS Letters, 486, 131-135 (2000)
» リフォールディング例の詳細情報はこちら 36KB
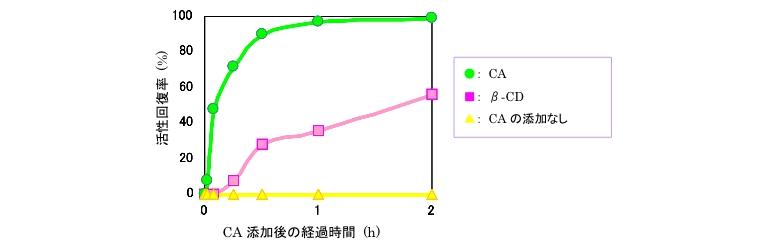
<3>シクロアミロースによるCitrate Synthaseの活性回復の経時変化
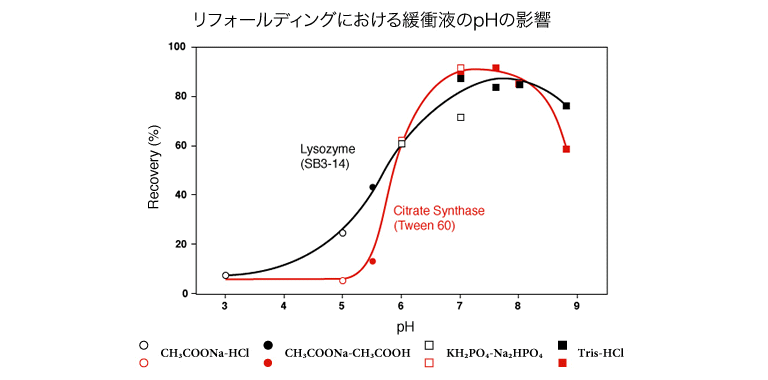
<4>リフォールディングにおける緩衝液のpHの影響
リフォールディングの実験結果は、用いる緩衝液の種類やpHにより影響を受けます。下図は、lysozymeおよびcitrate synthaseのリフォールディングにおいて、緩衝液の種類を変えて行った結果です。このように本手法では、界面活性剤液に使用する緩衝液の種類に影響を受けることが分かります。
リフォールディングの条件は、タンパク質ごとに異なると考えられますが、望ましいリフォールディング結果が得られない場合には、緩衝液の種類を変化させることにより、よい結果が得られる可能性があります。
<5>リフォールディング溶液からのタンパク質精製
本手法を用いてリフォールディングされたタンパク質溶液は、界面活性剤およびシクロアミロースを含んでいます。これらを、リフォールディング後の溶液から除去する必要がある場合には、以下の方法をお試しください。
界面活性剤の除去
リフォールディング溶液に、緩衝液で平衡化したBio Beads(Bio Rad社)を1/5容量加え、2時間混合後、遠心により上清を回収します。この操作により、通常CTABの99%、SB3-14の90%以上が除去されます。Tween40、Tween60についても、この方法である程度除去できます。シクロアミロースの除去
リフォールディング溶液中のシクロアミロースをさらに除去する必要がある場合には、タンパク質精製用各種クロマトグラフィー樹脂が利用できます。代表的なクロマトグラフィー樹脂に対する、シクロアミロースの挙動を以下に示します。
-各種クロマトグラフィー樹脂に対するシクロアミロースの挙動-
| 陰イオン交換樹脂Q sepharose、DEAE sepharose(Amersham Bioscience) |
吸着しません。*1 |
| 陽イオン交換樹脂SP sepharose、CM sepharose(Amersham Bioscience) |
吸着しません。*1 |
| 疎水吸着樹脂 Phenyl sepharose、Butyl sepharose(Amersham Bioscience) Octyl sepharose(Amersham Bioscience) |
吸着しません。 *1 弱く吸着します。 *2 |
| ゲルろ過樹脂 Sephadex G25(Amersham Bioscience) Superdex 30(Amersham Bioscience) |
分子量5,000~7,000のデキストリンと同じ溶出挙動を示します。 牛血清アルブミン(BSA)と同じ位置に溶出されます。 BSAよりやや遅れて溶出されます。 |
*1:2 bed volumeの洗浄で95%以上のCAが溶出されます。
*2:2 bed volumeの洗浄では80%、5 bed volumeの洗浄で90%以上のCAが溶出されます。
<6>リフォールディング用シクロアミロースの重合度および平均分子量
重合度約30(分子量4,900)のシクロアミロースを中心として、分子量3,600~8,000(重合度22~50)に分布するシクロアミロースの混合物で、平均分子量は約7,000(SEC-MALLS法による測定より)です。
サンプル依頼およびお問い合わせ
サンプルのご依頼や商品に関するお問い合わせを受け付けております。
■電話でのお問い合わせ
| お問い合わせ先 | グリコ栄養食品株式会社 技術営業部 〒555-8502 大阪市西淀川区歌島4-6-5 TEL.06-6477-8281 |
| 試薬に関するお問い合わせ | 富士フイルム和光純薬株式会社 〒540-8605 大阪市中央区道修町3-1-2 TEL.06-6203-3741 |
■メールでのお問い合わせ